干貨PPT速覽 醫(yī)療器械產(chǎn)品開發(fā)與網(wǎng)絡技術融合全流程解析
醫(yī)療器械產(chǎn)品開發(fā)是一個高度嚴謹且受法規(guī)嚴格監(jiān)管的過程。隨著網(wǎng)絡技術的飛速發(fā)展,物聯(lián)網(wǎng)、大數(shù)據(jù)、人工智能等新技術正深度融入醫(yī)療器械的開發(fā)周期,推動行業(yè)向智能化、遠程化、個性化方向轉型。以下結合PPT干貨內容,系統(tǒng)梳理醫(yī)療器械產(chǎn)品開發(fā)與網(wǎng)絡技術融合的關鍵流程。
一、需求分析與概念定義階段
此階段核心是明確臨床需求與產(chǎn)品定位。網(wǎng)絡技術的介入,使得開發(fā)團隊能通過大數(shù)據(jù)分析海量臨床數(shù)據(jù)、電子病歷和公開研究,更精準地識別市場缺口與用戶痛點。例如,通過分析可穿戴設備收集的連續(xù)生理參數(shù),可為慢性病管理設備開發(fā)提供明確方向。概念定義需同步考慮產(chǎn)品的網(wǎng)絡功能屬性,如數(shù)據(jù)連接方式(藍牙、Wi-Fi、5G)、云平臺架構及網(wǎng)絡安全基線。
二、法規(guī)路徑規(guī)劃與設計輸入
醫(yī)療器械開發(fā)必須遵循各國法規(guī)(如中國NMPA、美國FDA、歐盟MDR)。集成網(wǎng)絡技術的軟件(如嵌入式軟件、獨立醫(yī)療軟件SaMD)成為監(jiān)管重點。開發(fā)團隊需在早期明確產(chǎn)品的網(wǎng)絡技術組件所屬的合規(guī)類別(如網(wǎng)絡安全、數(shù)據(jù)隱私GDPR/HIPAA、互操作性標準),并將其作為關鍵設計輸入。設計輸入文檔需詳細定義功能、性能、接口及網(wǎng)絡安全要求(如數(shù)據(jù)加密、訪問控制、安全更新機制)。
三、詳細設計與技術開發(fā)
此階段將概念轉化為具體技術方案。硬件設計需考慮網(wǎng)絡模塊的集成(如低功耗芯片、天線設計)。軟件開發(fā)成為重心,包括:
- 嵌入式開發(fā):實現(xiàn)設備端的網(wǎng)絡連接、數(shù)據(jù)采集與本地處理。
- 云端與后端開發(fā):構建安全可靠的云平臺,用于數(shù)據(jù)存儲、分析、可視化及遠程管理。微服務架構、API設計是關鍵。
- 移動端/Web端應用開發(fā):提供用戶(醫(yī)護或患者)交互界面。
- 網(wǎng)絡安全貫穿始終:實施威脅建模、安全編碼、漏洞測試,確保數(shù)據(jù)在傳輸與存儲中的機密性、完整性和可用性。
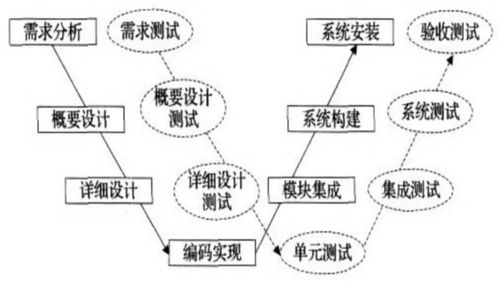
四、原型構建與設計驗證
制作集成網(wǎng)絡功能的工程原型,通過嚴格的測試驗證設計是否滿足輸入要求。測試重點包括:
- 功能與性能測試:網(wǎng)絡連接穩(wěn)定性、數(shù)據(jù)傳輸速率與延遲、多設備并發(fā)能力。
- 網(wǎng)絡安全測試:滲透測試、漏洞掃描、數(shù)據(jù)加密驗證。
- 互操作性測試:與醫(yī)院信息系統(tǒng)(HIS、EMR)或其他設備的標準接口(如HL7、FHIR、DICOM)對接測試。
五、設計確認與臨床評價
通過臨床評價(可能包括臨床試驗)確認產(chǎn)品在真實使用環(huán)境下的安全有效性。網(wǎng)絡技術在此階段發(fā)揮巨大價值:遠程監(jiān)控功能可簡化臨床試驗數(shù)據(jù)收集;真實世界數(shù)據(jù)(RWD)可作為臨床證據(jù)的補充。必須驗證網(wǎng)絡功能在臨床場景下的可靠性與安全性。
六、注冊申報與質量管理體系
整理技術文檔,提交監(jiān)管機構注冊/申報。對于含網(wǎng)絡技術的產(chǎn)品,需額外提交網(wǎng)絡安全文檔、架構描述、風險控制措施等。整個開發(fā)過程必須在完善的質量管理體系(如ISO 13485)下進行,確保開發(fā)過程可追溯、可控制。軟件生命周期過程需遵循IEC 62304標準。
七、生產(chǎn)轉移與上市后監(jiān)管
產(chǎn)品獲批后,轉入規(guī)模化生產(chǎn)。網(wǎng)絡技術部分(特別是軟件)需建立持續(xù)維護機制,包括:
- 遠程監(jiān)控與維護:通過網(wǎng)絡對已部署設備進行狀態(tài)監(jiān)控、故障診斷和軟件更新。
- 網(wǎng)絡安全漏洞管理:建立應急響應機制,持續(xù)監(jiān)控和修補新發(fā)現(xiàn)的安全漏洞。
- 數(shù)據(jù)迭代與產(chǎn)品優(yōu)化:利用收集的匿名化大數(shù)據(jù),分析產(chǎn)品性能,為下一代產(chǎn)品開發(fā)提供洞察。
****
網(wǎng)絡技術已深度嵌入醫(yī)療器械產(chǎn)品開發(fā)的全鏈條,從需求洞察到上市后生命周期管理。成功的開發(fā)需要跨學科團隊(醫(yī)學、工程、軟件、網(wǎng)絡安全、法規(guī))緊密協(xié)作,并始終將網(wǎng)絡安全、數(shù)據(jù)隱私和法規(guī)合規(guī)置于核心地位。擁抱網(wǎng)絡技術,不僅能開發(fā)出更智能、高效的醫(yī)療器械,更能構建以數(shù)據(jù)為驅動的連續(xù)健康服務生態(tài)。
如若轉載,請注明出處:http://www.jwyb168.com/product/79.html
更新時間:2026-05-09 08:23:24